Prospettive
 La terapia cellulare attuale per la distrofia muscolare può essere ottenuta sia usando cellule satellite o uno dei precursori cellulari non ortodossi citati in precedenza, le cui caratteristiche positive devono essere valutate attentamente.
La terapia cellulare attuale per la distrofia muscolare può essere ottenuta sia usando cellule satellite o uno dei precursori cellulari non ortodossi citati in precedenza, le cui caratteristiche positive devono essere valutate attentamente.
Quando possibile, le cellule devono essere derivate dallo stesso paziente (autologhe) o da un donatore sano (eterologhe): nel primo caso il gene difettivo deve essere corretto o sostituito per rendere il trapianto efficace; nel secondo caso la correzione del difetto genico non è necessaria ma il paziente deve essere sottoposto a terapia immunosoppressiva per prevenire il rigetto di cellule estranee.
In entrambi i casi, per ottimizzare le probabilità di successo delle cellule staminali per la terapia della distrofia muscolare è necessario a) isolare le cellule da un sito anatomico accessibile; b) crescerle in laboratorio senza la perdita della capacità di automantenersi e di generare cellule muscolari differenziate; c) introdurre efficientemente il gene riparato (per le cellule autologhe); d) raggiungere il muscolo malato attraverso la circolazione del sangue.
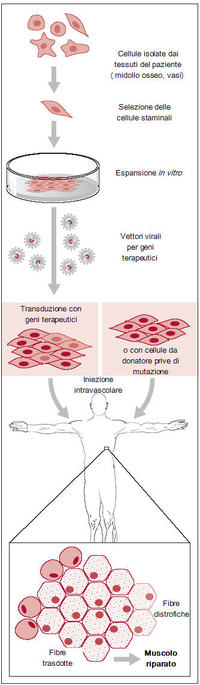
Uno schema teorico di questo processo è illustrato nella figura 1. Le cellule possono essere isolate da biopsie del muscolo scheletrico (cellule satellite ma anche vasi), tessuto adiposo, midollo osseo, sinovie e derma.
Le cellule satellite derivate dai pazienti affetti da DMD dovrebbero essere, ovviamente, la prima scelta ma esistono dei problemi che seriamente ostacolano questa strada: sono già esaurite nei pazienti con DMD, non possono attraversare la parete dei vasi – quindi non possono essere introdotte per via sistemica – e, inoltre, non possono migrare dal sito dell’iniezione intramuscolare, per cui richiedono migliaia di iniezioni.
Per tutti gli altri tipi cellulari è imperativo fornire evidenze di differenziamento efficiente in tessuto muscolare in vivo e in vitro, dopo il trapianto in topi distrofici immunodeficienti. Per i progenitori miogenici non standard, ci sono evidenze recenti di efficacia da uno studio che utilizza precursori associati ai vasi nei modelli murini di distrofia muscolare dei cingoli (5). Più di recente, è stato dimostrato che le cellule umane dal tessuto adiposo e dal midollo osseo possono ricostruire il muscolo nei topi distrofici, ma l’estensione della ricostruzione resta da valutare.
La ricerca sulle cellule staminali probabilmente chiarirà maggiormente l’identità, le caratteristiche biologiche e la relazione tra le linee delle cellule satelliti e di altri precursori cellulari non tipici del muscolo.
Nel contempo, i protocolli di terapia cellulare - con benefici derivanti dalla corrente ricerca di base – sono applicati in animali più grandi, come i cani distrofici. Questo metterà a punto (forse in un paio di anni) le linee per i trial clinici in pazienti distrofici. Inevitabilmente, all’inizio i risultati saranno modesti (miglioramenti, più che cure), perché il metodo richiede ottimizzazione. Nei prossimi cinque – dieci anni, se saranno disponibili fondi appropriati (le distrofie muscolari sono rare e di scarso interesse per le aziende), l’ottimizzazione dei protocolli migliorerà il risultato clinico e una cura completa di questa malattia intrattabile e devastante potrebbero essere a vista.
- A meno che non sia risolto il problema del numero limitato di cellule satelliti, i migliori candidati per il trattamento della distrofia muscolare di Duchenne sembrano essere altre cellule staminali mesodermiche, sia residenti nel muscolo o (meno probabilmente) derivate da altri tessuti.
- L’origine di queste cellule, la loro relazione con le cellule satellite, la caratterizzazione e l’abilità di formare muscolo scheletrico dovrebbero essere approfonditi per valutare meglio la loro utilità per la terapia.



